质谱分析长期以来一直受制于其固有的“串行”逻辑——无论前端分离得多好,离子在进入分析器后总需要排着队被逐一挑选和碎裂。当我们面对蛋白质组学或代谢组学中复杂如海的样本、却又想观测其中不明确的目标时,它们时常被淹没在背景噪音中,不可避免地遭遇灵敏度与动态范围的瓶颈。
近期,洛克菲勒大学的 Andrew N. Krutchinsky 和 Brian T. Chait 在《Science Advances》上发表的 MultiQ-IT (Multi-Quadrupole Ion Trap) 技术,提供了一种打破常规的硬件解法。链接:https://www.science.org/doi/epdf/10.1126/sciadv.aec7048

媲美细胞核的仿生学离子阱设计
传统离子阱,无论是三维阱还是线性阱,都只有单一的进出口,必须依赖依次累积、冷却、再脉冲式排出的时间顺序操作。相比之下,MultiQ-IT 的设计灵感极其巧妙,直接借鉴了细胞的核质运输机制。细胞核通过表面有限数量的核孔复合体实现高效的分子交换;MultiQ-IT 也有样学样,通过排列大量微小四极杆构建了一个立方体阵列,形成了至多上千个并行的离子出入通道。
在这个阵列中,离子不再依靠复杂的电场聚焦来排队,而是通过热扩散这一基础物理过程在腔室内运动。由于突破了单一出口的空间电荷限制,该系统每秒可以容纳并处理超过 10^9 个离子,这比 Q Exactive HF 等质谱仪常规装配的离子阱容量高出了三个数量级。
实验表现
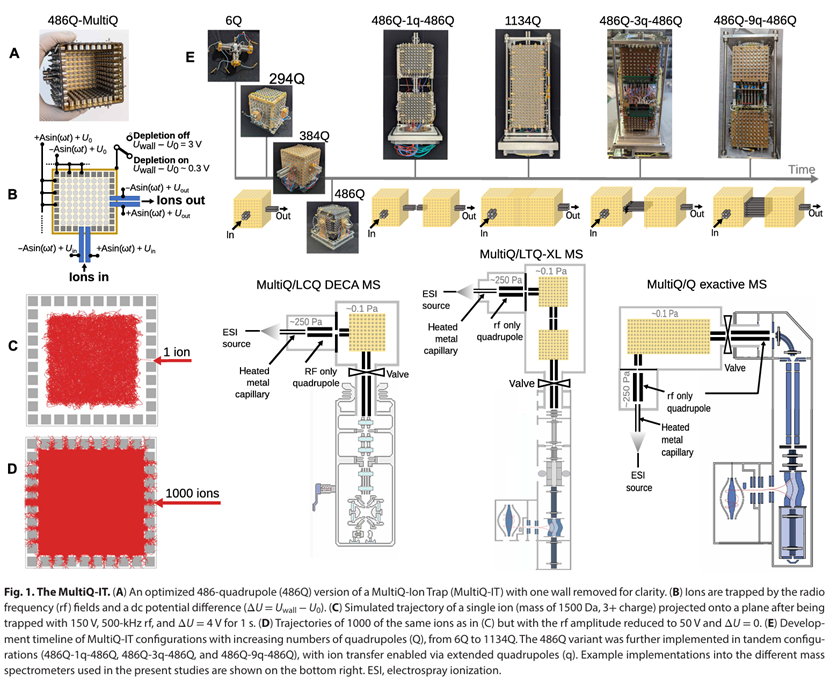
实时电荷分离:通过调节四极杆出入口与外壁间微小的电势差(文中给出了3V的屏障电压为例子),系统能精确控制不同电荷离子的逃逸概率。在离子穿过阱的瞬间,单电荷的化学噪音离子会优先越过低电势垒并被消耗掉,这完全不需要传统的脉冲冷却步骤。实验表明,在串联使用两个 486Q 阱后,复杂肽段混合物的信噪比获得了约 100 倍人提升。
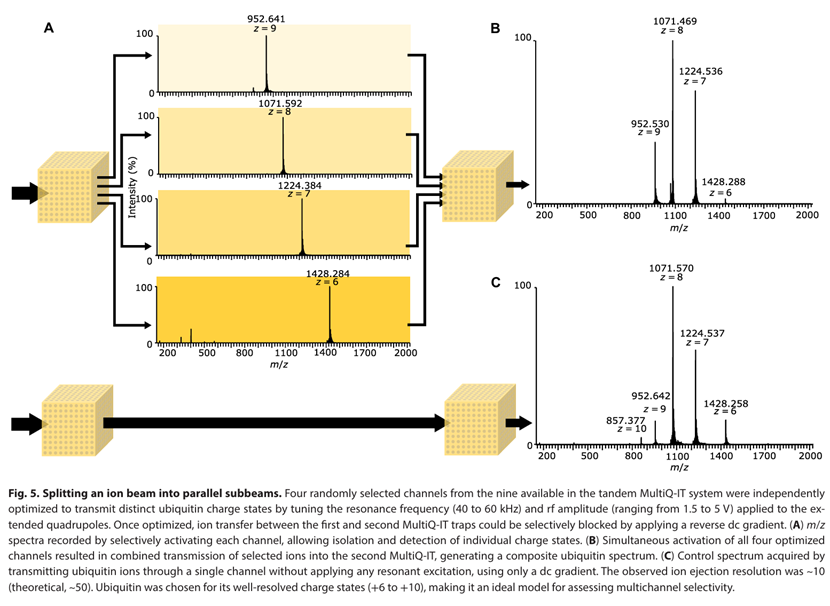
大规模并行的离子分束:MultiQ-IT 还可以作为分流器,通过对特定出口通道施加共振频率激发,将一束混合离子同时拆分成多个具有特定质荷比范围的子光束。这意味着,非共振的离子会被弹回阱内继续寻找自己的“专属通道”,而选定的多束离子可以同时进入下游的并行质量分析器中。这为未来打造拥有多个同时运作分析通道的质谱仪奠定了硬件概念基础。
高吞吐质谱检测的闭环
基于质谱的组学正迎来高吞吐量的黄金年代。这项 MultiQ-IT 技术是在质谱设备内部解决了分析物“检票入场”的瓶颈,而去年发表的 SynchroSep-MS 则在质谱前端解决了液相分离“排队”的问题(链接:https://pubs.acs.org/doi/10.1021/jasms.5c00207),数年前的 CellenONE、AccelerOme、PreOmics 等技术则在实验台上搞定了样本制备“排队”的问题。通过极度压缩周转时间、榨干仪器分析效率,高吞吐检测的未来蓝图似乎正在实现全链条闭环。
高吞吐与高通量
多项报道对比和赞誉先进质谱技术带来的通量提升。然而,笔者认为,必须厘清“高吞吐”与“高通量”的本质区别。即使在 MultiQ-IT 等多种技术赋能后,质谱仍主要体现前者的特征,而非后者。这根本上是由其检测的物理逻辑决定的。
质谱直接检测分析物离子本身,每个信号(谱峰)对应一个或一群真实的离子。虽然像 MultiQ-IT 可以并行处理更多离子、像DIA等技术可以提升离子利用率、像 FAIMS 或 TIMS 等装置可以提升信噪比,但它无法改变 “一个离子产生一个有限信号” 的物理本质。其通量提升是“线性”或“多项式级”的优化,通过更高效的利用和更快的循环来实现。
与之形成鲜明对比,以NGS为代表的高通量技术,其核心是对间接的、可扩增的信号进行并行读取。NGS 通过 PCR 对数百万个 DNA 模板进行指数级扩增,从而能够检测来自这些克隆集群的强信号。这种基于信号扩增的并行读取机制,使其能够同时对海量模板进行测序,从而实现真正意义上的高通量:一次运行完成数百万至数十亿个检测。
因此,MultiQ-IT 等技术的革命性在于,它们是在质谱技术的物理极限内,通过架构创新将分析效率与深度推向极致。它们旨在解决“在有限时间内,尽可能多、尽可能好地捕获和利用每一个珍贵的离子”这一核心挑战。其目标并非在“数据产出速率”上与 NGS 竞争,而是在其擅长的 “对复杂混合物进行深度、定量、无偏向性的直接分子鉴定” 这一独特赛道上,不断突破现有的性能天花板。高吞吐是质谱走向更深、更快的必由之路,但高通量或许是它物理原理上永远无法抵达的彼岸。